Натуральные гепатопротекторы: ТОП-5 защитников печени

Натуральные гепатопротекторы: ТОП-5 защитников печени
Не зря природа наделила печень способностью к самовосстановлению. Но все же ее ресурсы не безграничны, и поэтому обеспечение дополнительной защиты печени – наш с вами долг. Помощь в этом могут оказать натуральные гепатопротекторы.
Как работают натуральные гепатопротекторы
К натуральным гепатопротекторам относятся препараты растительного и животного происхождения, которые способствуют:
- повышению устойчивости клеток печени к повреждающим воздействиям;
- нормализации важнейших функций печени, в том числе способности нейтрализовать токсины;
- снижению выраженности воспаления;
- восстановлению поврежденных клеток печени.
Алкоголь и курение, несбалансированное питание, бесконтрольное применение лекарств, инфекции, частые стрессы… Наша печень вынуждена отражать атаку за атакой. Кстати говоря, недавно ученые выяснили, что признаки ее поражения могут отмечаться при новой коронавирусной инфекции COVID-19.
Какой гепатопротектор выбрать
А теперь мы составим свой рейтинг гепатопротекторов и расскажем об особенностях действия каждого из них.
Эссенциальные фосфолипиды
Если вас интересуют гепатопротекторы с доказанной эффективностью, то эссенциальные фосфолипиды – один из топовых препаратов. История их изучения насчитывает более 50 лет, и за это время они доказали свою эффективность и безопасность.
Эссенциальные – значит существенные, необходимые. И к фосфолипидам это определение полностью подходит, ведь они являются одним из ключевых компонентов мембран гепатоцитов – печеночных клеток.
Эссенциальные фосфолипиды натурального происхождения в составе препаратов идеально близки собственным фосфолипидам организма. Они «находят» повреждения в клеточных мембранах и встраиваются в них, благодаря чему восстанавливается структура и функции гепатоцитов.
Также эссенциальные фосфолипиды способствуют замедлению процесса накопления жира и снижению активности воспаления в печени, улучшению работы митохондрий – «энергетических станций» клеток, повышению детоксикационной функции печени.


Куркумин
Это активное вещество «золотой специи» куркумы, которое, как талантливый актер, способно играть много ролей, в том числе роль мощного гепатопротектора. Исследования с участием пациентов с «ожирением» печени показали, что куркумин способствует снижению содержания жира в ее клетках. А при изучении защитных свойств куркумина на животных выяснилось, что он улучшает структуру печени, активно борется с окислительным стрессом и подавляет воспалительные процессы.
Кроме того, куркумин называют «натуральным антибиотиком» с антибактериальными, противовирусными и противогрибковыми свойствами. И это большой плюс, ведь инфекции часто наносят удар по печени.
«А вот я обожаю куркуму!» — скажете вы. Отлично! Только помните об одном «НО»! Из самой специи куркумин очень плохо усваивается. К счастью, ученые научились получать биодоступный куркумин, переводя его в мицеллярную форму. Такой куркумин усваивается на отлично – практически полностью.


Расторопша
В группе «растительные гепатопротекторы» это растение, несомненно, в самом топе. А точнее, экстракт из плодов расторопши – силимарин. Его способность защищать клетки печени от влияния негативных факторов (токсины, вирусы, радиация и т.д.) подтверждается результатами клинических исследований.
Силимарин действует сразу в нескольких направлениях:
- «обезоруживает» свободные радикалы и препятствует истощению запасов антиоксиданта глутатиона,
- улучшает детоксикационную функцию печени,
- проявляет противовоспалительные свойства,
- препятствует проникновению токсинов в клетки печени и оказывает защитное действие на их мембраны,
- стимулирует процессы естественного самовосстановления в печени путем повышения синтеза белка.
Интересный факт!
При отравлении бледной поганкой силимарин препятствует проникновению ядов этого гриба в клетки печени и тем самым снижает степень ее токсического поражения.
Впрочем, отравление грибами — очень опасное состояние, поэтому в любом случае попытки самолечения недопустимы!



Артишок
«Ни дня без артишока!» Такой поговоркой, широко известной в Древнем Риме, Плиний Старший охарактеризовал одно из гастрономических пристрастий своих современников. А для нас сегодня артишок представляет ценность не только как кулинарный деликатес, но и замечательный гепатопротектор.
Артишок отличается высоким содержанием белков, углеводов, витаминов С, В2, В6, каротина, минералов, ароматических веществ и других компонентов, благодаря которым способствует восстановлению клеток печени и улучшению ее работы. Как и многие другие натуральные гепатопротекторы артишок повышает антиоксидантную защиту мембран клеток печени и ее детоксикационную функцию, помогает выводить из организма различные токсины, соли тяжелых металлов, радионуклиды, обладает желчегонным действием.
Печеночная энцефалопатия (гепатоэнцефалопатия)
Печеночная энцефалопатия (гепатоэнцефалопатия)
Печеночная энцефалопатия (гепатоэнцефалопатия) — потенциально обратимое расстройство нервной системы, обусловленное метаболическими расстройствами, возникающими в результате печеночно-клеточной недостаточности и/или портосистемного шунтирования крови.
Механизмы появления и развития печеночной энцефалопатии на сегодняшний день остаются неясными. Обычно наблюдается сложный комплекс нарушений, ни одно из которых не дает исчерпывающего объяснения. Известно, что заболевание развивается при ряде синдромов – острой печеночной недостаточности, циррозе печени, липидозе печени у кошек, врожденных портоковальных анастомозов, важную роль играет также печеночно-клеточная (паренхиматозная) недостаточность.
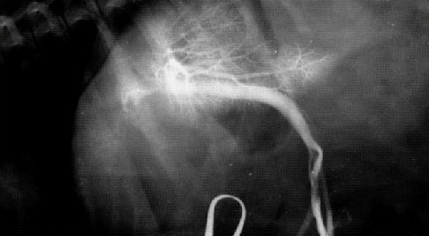
Рис.1. У таксы в возрасте 2-х лет асцит, гипертрофия правой доли печени, отсутствие кровотока в правой медиальной и левой латеральной доли.
Хроническая гепатоэнцефалопатия наблюдается у больных животных с портокавальным шунтированием или с патологией портальной вены (гепатопортальная микроваскулярная дисплазия). (Рис.1).
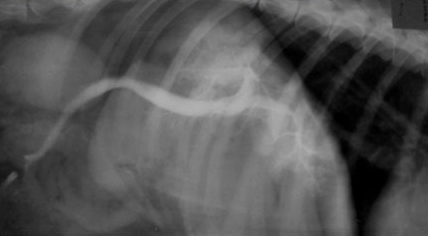
Рис.2.На снимке нарушение портального кровотока у собаки породы тоса-ину.
Различные симптомы печеночной энцефалопатии, вероятно, отражают количество и тип образующихся метаболитов. Кома при острой печеночной недостаточности часто сопровождается психомоторным возбуждением и отеком мозга. Для печеночной энцефалопатии характерны заторможенность и сонливость, иногда понижение температуры тела, повреждение астроцитов, нарушение гематоэнцефалического барьера, что в свою очередь может привести к осложнениям воспалительного характера в центрольной нервной системе.
Клиническая картина
При печеночной энцефалопатии поражаются практически все отделы головного мозга, поэтому клиническая картина представляет собой комплекс различных синдромов, включающих в себя неврологические и психические нарушения.
Разнообразие клинических симптомов при гепатоэнцефалопатии связано с повреждением глутаматных рецепторов. Глутамат синтезируется в нейронах из своего предшественника глутамина, накапливается в синаптических везикулах и в итоге высвобождается при помощи кальций-зависимого механизма. Высвободившийся глутамат может взаимодействовать с глутоматными рецепторами любого типа, находящимися в синаптической щели. В астроцитах под действием глутаминсинтетазы из глутамата и аммиака синтезируется глутамин. Развивающееся при гепатоэнцефолопатии нарушения включают увеличение содержания аммиака в головном мозге, приводят к повреждению астроцитов, уменьшению числа глутаматных рецепторов. Гепатоэнцефалопатия может проявляться по-разному. Могут быть повышены глубокие сухожильные рефлексы и мышечный тонус на некоторых стадиях. Возможны судороги, мышечные подергивания, у некоторых пациентов нарушается координация движений, состояния ухудшается после приема пищи. Во время комы рефлексы ослаблены и постепенно исчезают. Наблюдаются вялость, сонливость, понижение температуры тела.
Исследование спинномозговой жидкости
Специфических изменений в ликворе при гепатоэнцефалопатии не обнаружено.
Возможно повышение глутамина.
Электроэнцефалография
При гепатоцеребральной дистрофии у большинства пациентов при ЭЭГ-исследовании наблюдаются изменения в виде медленных волн, могут быть высокоамплитудные дельта волны, эпилептическая активность. Этот метод помогает при диагностике печеночной энцефалопатии и оценке результатов лечения, особенно на ранних этапах до появления клинических симптомов. Они неспецифичны и могут проявляться при других патологических состояниях, например при уремии.
Клинические варианты печеночной энцефалопатии
Острая энцефалопатия может развиться спонтанно под воздействием предрасполагающих факторов, особенно у больных с билирубинемией и асцитом после удаления большого количества жидкости, что, по-видимому, связано с потерей воды и электролитов. Богатая белками пища или длительные запоры могут способствовать развитию комы, а угнетение функции печеночных клеток вызвано анемией и снижением печеночного кровотока.
Пациенты с острой энцефолопатией плохо переносят хирургические операции, поскольку из-за кровопотери, анестезии и шока происходит усугубление нарушений функции печени. Развитию печеночной энцефолопатии могут способствовать инфекционные заболевания особенно в тех случаях, когда они осложняются бактериемией.
Хроническая энцефалопатия
Развитие хронической гепатоэнцефолопатии обусловлено значительным портосистемным шунтированием. Шунты могут быть врожденными (наиболее часто встречаются у йоркширских терьеров), приобретенными, могут состоять из множества мелких анастомозов, развившихся у больного циррозом печени или из крупного коллатерального сосуда. Выраженность гепатоэнцефолопатии зависит от содержания белка в пище. В этом случае постановка диагноза может вызвать затруднения. Диагноз становится очевидным, если при переходе на низкобелковую диету состояние пациента улучшается.
Данные энцефалографии могут помочь в постановке диагноза.
Гепатоцеребральная дегенерация ( Миелопатия) развивается после длительной хронической печеночной энцефолопатии и связана с очаговыми повреждениями головного мозга. Могут наблюдаться эпилептические припадки, нарушение двигательной функции, развиться синдром поражения мозжечка и базальных ядер мозга.
Патогенез
Метаболическая теория развития гепатоэнцефолопатии основывается на обратимости ее основных расстройств при обширных церебральных нарушениях. Не существует единственного метаболического нарушения, вызывающего гепатоэнцефолопатию.
В основе ее лежат снижение печеночного клиренса образующихся в кишечнике веществ как вследствие печеночно-клеточной недостаточности, так и за счет значительного шунтирования, а также нарушение метаболизма аминокислот. Оба эти механизма ведут к нарушениям в церебральных нейротрансмиттерных системах.
В патогенезе гепатоэнцефолопатии участвуют несколько нейротоксинов, особенно аммиак, и несколько нейромедиаторных систем, взаимодействующих между собой.
У каждого больного, находящегося в состоянии комы или прикомы, кровь может попадать из воротной вены в системные вены, минуя печень и не проходя детоксикацию.
У больных с нарушением функции гепатоцитов, например при остром гепатите, кровь шунтируется внутри печени. Поврежденные гепатоциты не в состоянии в полной мере проводить детоксикацию крови портальной системы, поэтому кровь поступает в печеночные вены с токсинами. При циррозе кровь из воротной вены минует печень по большим естественным коллатералям, поступает в системные вены. Кроме того, в пораженной циррозом печени вокруг долек образуются портопеченочные венозные анастомозы, которые функционируют как внутрипеченочные шунты.
Аммиак и глутамин
В патогенезе гепатоэнцефалопатии аммиак — наиболее изученный фактор. Аммиак выделяется при расщеплении белков, аминокислот, пуринов и пиримидинов. Около половины аммиака, поступающего из кишечника, синтезируется бактериями, а оставшаяся часть образуется из белков пищи и глутамина. В норме в печени аммиак превращается в мочевину и глутамин. Нарушение цикла мочевины ведут к развитию энцефолопатии. Уменьшение количества мочевины в крови может служить показателем развивающейся гепатоэнцефолопатии. Уровень аммиака повышен в крови у 90% пациентов. Содержание его в головном мозге может быть тоже увеличено. При пероральном получении солей аммония у некоторых больных может развиться гепатоэнцефолопатия.
Сама по себе гипераммониемия связана со снижением проведения возбуждения в ЦНС. Интоксикация аммиаком ведет к развитию гиперкинетического предсудорожного состояния. При гепатоэнцефолопатии основные механизмы действия аммиака заключаются в прямом воздействии на мембраны нейронов или на постсинаптическое торможение и в опосредованном нарушении функций нейронов в результате влияния на глутаматергическую систему.
Роль глутамата в центральной нервной системе
L-глутамат — главный возбуждающий медиатор в мозге животных. Глутамат обнаруживается во всех отделах ЦНС, т.к. он является не только нейромедиатором, но и предшественником других аминокислот. Тела глутаматергических нейронов находятся в коре больших полушарий, обонятельной луковице, гиппокампе, черной субстанции, мозжечке, сетчатке. Глутаматергические синапсы существуют в миндалине, стриатуме, на клетках-зернах мозжечка. Основные нисходящие пути идут от пирамидных клеток новой коры и гиппокампа. Эти тракты включают в себя кортиокстриарный, энторинально-гиппокампальный, а также гиппокампальные и корковые пути к различным гиппокампальным, таламическим и стволовым ядрам.
Глутамат — заменимая аминокислота, не проникает через ГЭБ, не поступает в мозг через кровь. Синтез осуществляется в мозге, в основном внутринейронально, хотя малая доля общего пула глутамата находится в астроцитах. Глутамат может быть синтезирован из альфа-кетоглутарата путем прямого восстановительного аминирования или трансаминирования, из глутамина (катализатор — глутаминаза), а также из орнитина (катализатор — орнитинаминотрансфераза).
Синтез глутамата из альфа-кетоглутарата катализируется глутаматдегидрогеназой: aльфа-кетоглутарат + NADH(NADPH)+NH3 глутамат + H2O + NAD+(NADP+)
Синтез глутамата из глутамина катализируется глутаминазой, локализованной в митохондриях. Активность этого фермента в мозге невелика, но предполагается участие его в мембранном транспорте глутамата (биологические мембраны более проницаемы для глутамина). Глутаминаза играет важную роль в регуляции содержания глутамата в нервных окончаниях (Ашмарин и др., 1999).
Помимо основной роли возбуждающего нейромедиатора, глутамат может проявлять нейротоксические свойства. При гиперактивации глутаматергической передачи происходит интенсивное поступление ионов кальция в клетку. Повышенное содержание свободного кальция способно индуцировать процессы образования реактивных форм кислорода. Следствием этих процессов может стать повреждение и гибель нейронов.
Глутаматсвязывающая активность обнаружена практически во всех структурах мозга. Наибольшее количество участков связывания находится в коре больших полушарий, гиппокампе, стриатуме, среднем мозге и гипоталамусе.
Глутаматные рецепторы подразделяются на ионотропные и метаботропные. Существует несколько подтипов глутаматных рецепторов. Современная класификация ионотропных рецепторов основана на разной их чувствительности к действию N-метил-D-аспарагиновой (NMDA), 2-амино-3(3-гидрокси-5-метилизоксазол-4-ил)пропионовой (АМРА), каинатной и квисквалатной кислот. Выделяют две группы рецепторов: NMDA и не-NMDA (их подразделяют на АМРА и каинатные).
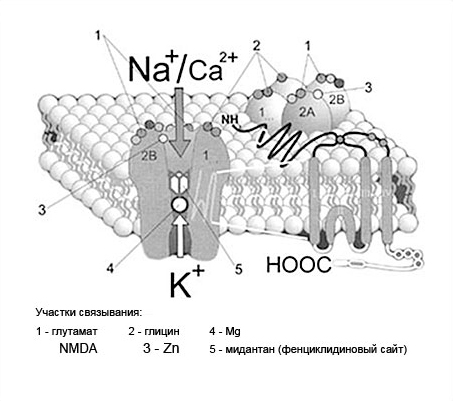
Рис.3. Структура NDMA-рецептора.
NMDA-рецепторы (рис.3) состоят из пяти субъединиц, по 40-92 кД каждая, (одной NMDAR1 и четырех NMDAR2A-NMDAR2D).
Эти субъединицы являются гликопротеидлипидными комплексами. Собственно, говоря, NMDA-рецептор представляет из себя целый рецепторно-ионофорный комплекс, включающий в себя:
1. сайт специфического связывания медиатора (L-глутаминовой кислоты);
2. регуляторный, или коактивирующий сайт специфического связывания глицина;
3. аллостерические модуляторные сайты, расположенные на мембране (полиаминовый) и в ионном канале (сайты связывания фенциклидина, двухвалентных катионов и потенциалзависимый Mg2+-связывающий участок).
NMDA-рецепторы обладают рядом особенностей: одновременно хемо- и потенциал-чувствительностью, медленной динамикой запуска и длительностью эффекта, способностью к временной суммации и усилению вызванного потенциала. Наибольшие ионные токи при активации агонистами возникают при деполяризации мембраны в узком диапазоне -30- -20 мВ (в этом проявляется потенциалзависимость NMDA-рецепторов)(Jose et al., 1996). Ионы Mg2+ селективно блокируют активность рецепторов при высокой гиперполяризации или деполяризации. Глицин в концентрации 0,1 мкМ усиливает ответы NMDA-рецептора, увеличивая частоту открывания канала. При полном отсутствии глицина рецептор не активируется L-глутаматом (Сергеев П. В и др., 1999).
NMDA-рецепторы и вовлечены в формирование долговременной потенциации (LTP). Известно, что NMDA-рецепторы играют важную роль в процессах обучения и памяти. Они участвуют в формировании долговременной потенциации в гиппокампе. Существуют данные о вовлечении NMDA-рецепторов в процессы пространственного обучения (Ahlander et al., 1999; Whishaw and Auer, 1989). Показано, что при системном введении неконурентный блокатор NMDA-рецепторов, МК-801, нарушает обучение в водном лабиринте(Gorter and de Bruin, 1992).
Большое внимание в настоящее время уделяется роли NMDA-рецепторов в развитии шизофрении. Предполагается, что протекание этого заболевания частично связано со снижением эффективности глутаматергической передачи. Так, блокада NMDA-рецепторов неконкурентным антагонистом фенцклидином приводила к возникновению симптомов этого заболевания. Нарушения функции NMDA-рецепторов коррелируют с мнестическими расстройствами и изменениями социального поведения, наблюдаемыми у больных шизофренией (Parsons et al., 1998).
Каинатные рецепторы осуществляют быструю глутаматергическую передачу, участвуют в пресинаптическом контроле высвобождения медиатора. АМРА-рецепторы также осуществляют быструю передачу и работают синергично с NMDA-рецепторами (Ozawa et al.,1998).
Метаботропные глутаматные рецепторы связаны с G-белковым комплексом и модулируют уровень продукции вторичных мессенджеров. Выделяют три группы рецепторов. Рецепторы группы I mGluR1 и 5 активируют фосфолипазу С, что ведет к активации внутриклеточных посредников: инозитолтрифосфатов, протеинкиназы С и ионов кальция. Рецепторы групп II и III mGluR2, 3 и mGluR4,6,7,8 реализуют сигнал, подавляя синтез цАМФ (Ашмарин и др.,1999).
В головном мозге цикл мочевины не функционирует, поэтому удаление из него аммиака происходит различными путями. В астроцитах под действием глутаминсинтетазы из глутамата и аммиака синтезируется глутамин. В условиях избытка аммиака запасы глутамата ( важного возбуждающего медиатара ) истощаются и происходит накопление глутамина. Содержание глутамина и альфакетаглутарата в спинномозговой жидкости коррелирует со степенью гепатоэнцефалопатии. Трудно оценить вклад аммиака в развитие гепатоэнцефолопатии, так как при этом состоянии наблюдается изменение в других нейромедиаторных системах. У 10% пациентов уровень аммиака нормальный. Производные метионина, особенно меркаптаны, вызывают гепатоэнцефалопатию, поэтому использование метионина в качестве лекарственного препарата недопустимо. Имеются данные, что при гепатоэнцефолопатии некоторые токсины, такие как аммиак, жирные кислоты, фенолы, меркаптаны, действуют как синергисты.
Ложные нейротрансмиттеры
При гепатоэнцефолопатии передача импульсов в катехоламиновых и допаминовых синапсах головного мозга подавляется аминами, образующимися под действием бактерий в кишечнике при нарушении метаболизма предшественников нейромедиаторов в головном мозге. Декарбоксилирование в кишечнике некоторых аминокислот ведет к образованию беттафенилэтиламина, тирамина и октопамина-ложных нейротрансмиттеров. Они замещают истинные нейромедиаторы. Изменение доступности предшественников медиаторов препятствует нормальной нейропередачи.
У больных с заболеваниями печени возрастает содержание в плазме ароматических аминокислот- тиразина, фенилаланина, триптофана, что обусловлено нарушением их дезаминирования в печени. Одновременно понижается содержание аминокислот с разветвленной цепью — валина, лейцина, изолейцина, связанное с увеличением их метаболизма в скелетных мышцах и почках в результате гиперинсулинемии, характерной для больных с хронической печеночной недостаточностью. Эти две группы аминокислот конкурируют за прохождение в головной мозг. Нарушение их соотношения в плазме позволяет ароматическим аминокислотам проникнуть через нарушенный гематоэнцефалический барьер. Высокий уровень фенилаланина в головном мозге приводит к подавлению синтеза допамина и образованию ложных нейротрансмиттеров: фенилэтаноламина и октопамина.
При заболеваниях печени повышается содержание триптофана в спинномозговой жидкости и головном мозге. Триптофан является предшественником нейромедиатора серотонина. Серотонин участвует в регуляции уровня возбуждения коры головного мозга и цикла сон-бодрствования. При гепатоэнцефолопатии наблюдаются другие нарушения метаболизма серотонина. Является ли нарушение в этой системе первичным дефектом, нуждается в дальнейшем изучении.
Тяжесть гепатоэнцефалопатии коррелирует с бензодиазепиновой активностью плазмы крови и мочи. В кале больных циррозом печени активность бензодиазепиновых соединений в пять раз выше. Повышение чувствительности к бензодеазипинам подтверждает участие этой нейромедиаторной системы в развитии гепатоэнцефалопатии.
Другие метаболические нарушения
При гепатоэнцефолопатии может развиться гипогликемия. По мере усугубления печеночной недостаточности наблюдается прогрессирующее нарушение обмена углеводов. Мозг при гепатоэнцефолопатии становится чувствителен к воздействию вредных факторов: опиатов, электролитных нарушений, сепсису, артериальной гипотензии, гипоксии, что не отмечается в норме. Ветеринарный врач должен обязательно учитывать это при проведении операций и введении в наркоз пациентов с таким заболеванием.
Лабораторная диагностика гепатоэнцефалопатии
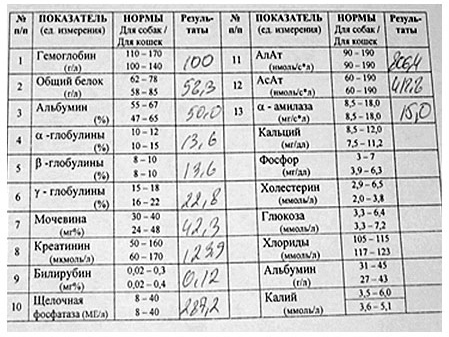
Биохимические и гематологические показатели, полученные в результате рутинных тестов, дают возможность лишь предполагать наличие гепатоэнцефалопатии. Наиболее полезными в этом отношении являются тест на концентрацию аммиака в крови, проверка толерантности к аммиаку, проверка содержания желчных кислот в сыворотке. Гематологические показатели у животных с гепатоэнцефалопатией не являются специфическими и могут включать слабую анемию, пойкилоцитоз, микроцитоз.
Подобно этому, изменения сывороточных концентраций биохимических показателей, ассоциированных с болезнями печени (АЛТ, ACT, альбумин, билирубин, глюкоза и калий), обычно не специфичны, сочетание низкого альбумина, низкой мочевины может говорить о наличии поражений печени, вызывающих гепатоэнцефалопатию. Концентрация в крови азота мочевины обычно очень низка (менее 6 мг/100 мл).
У животных с гепатоэнцефалопатией наблюдается дыхательный и метаболический алкалоз. Дыхательный алкалоз является вторичным по отношению к гипервентиляции, а метаболический алкалоз является результатом гипокалиемии и сильной рвоты.
Концентрация аммиака в крови обычно оценивается в образцах крови, взятой из артерии, и сыворотка должна быть отделена от клеток в течение 30 мин. Следует подчеркнуть, что степень серьезности неврологических признаков не всегда связана со степенью гипераммонизации. Некоторые энцефалопатические животные имеют нормальную концентрацию аммиака в крови, в то время как у других животных с минимальными неврологическими расстройствами наблюдается значительное повышение концентрации аммиака. Если повышенная концентрация аммиака (более 120 мкг/100 мл для собак) будет обнаружена спустя, по крайней мере, 6 часов после приема пищи, это будет иметь большое значение для постановки диагноза.
Для проверки толерантности к аммиаку измеряют разницу между величинами концентрации аммиака per os перед приемом и спустя 30 мин. после приема NH4Cl в дозе 100 мг/кг. Из-за риска вызвать гепатоэнцефалопатию эту проверку следует проводить осторожно и только на тех собаках, у которых неврологическое расстройство минимально, а концентрация аммиака нормальная и устойчивая. Для собак проверка толерантности к азоту может быть также выполнена путем ректального введения 5%-ного NH4Cl.
Концентрация аммиака в крови не является диагностическим показателем гепатоэнцефалопатии у кошек, поскольку у этих животных отсутствует способность синтезировать аргинин, который участвует в детоксикации аммиака в печеночном цикле Кребса-Гесельстайна. Более того, у кошек с длительной анорексией иногда наблюдается повышенная концентрация аммиака в крови. Принудительный прием аммиака per os, проведенный на кошке с устойчиво высокой концентрацией аммиака в крови, может вызвать у животного гепатоэнцефалопатию, кому и даже привести к гибели животного.
Концентрация сывороточных желчных кислот, измеренная натощак и спустя 2 часа после приема корма, считается безопасной и в равной степени достоверной проверкой для оценки функции клеток печени (см. Таблицу). Кроме того, никакой особой обработки образцов не требуется, поскольку сами они относительно стабильны. Концентрация желчных кислот в крови является очень полезным показателем для постановки диагноза гепатоэнцефалопатии у кошек.
Таблица. Общее содержание желчных кислот в сыворотке (нормальные значения для собак и кошек в мкмол/л)
| Натощак | Через 2 часа после приема корма | |
| Собака | 5 | 15-20 |
| Кошка | 4 | 10-15 |
По концентрации сывороточных желчных кислот нельзя дифференцировать болезни печени, однако, если их концентрация после приема корма сильно возрастает (более 150 ммол/л), то можно предполагать наличие цирроза или PSS. В большинстве лабораторий для определения концентрации желчных кислот в крови используют либо ферментный метод, с помощью которого измеряют общее содержание сывороточных 3альфа-гидроксилированных желчных кислот; либо радиоиммунный анализ (RIA), с помощью которого измеряют остатки специфических желчных кислот.
Рентгенография
Для всех случаев гепатоэнцефалопатии необходимо получить рентгеновские снимки брюшной полости. Печень у кошек и собак с гепатоэнцефалопатией может быть маленьких, увеличенных и даже нормальных размеров. Для идентификации как внутри, так и вне печеночного шунта, а также гепатопортальной микроваскулярной дисплазии можно использовать такие виды исследования, как спленопортографию, портографию через вену тощей кишки, портографию через краниальную брыжеечную артерию.
Наиболее предпочтительным является метод портографии через брыжеечную вену. После вентрального разреза по средней линии вокруг петли вены тощей кишки помещаются две лигатуры, катетер вставляется в сосуд и закрепляется.
Недопустимо использование металлической иглы.
Разрез брюшной полости временно закрывается. В катетер вводится соответствующее контрастное вещество, после чего проводится рентгеноскопия или рентгенография в латеральном и вентродорсальном направлениях. В качестве контраста используются омнипак 300 или 350 ,ультравист 370. Возможно использование урографина 70%, но нежелательно из-за возможных реакций на этот препарат у животных.
Доза омнипака для получения качественного изображения варьирует от 1 мл на кг веса у крупных собак до 2.5 мл на кг у мелких собак и кошек. Рентгеновский снимок делается в момент прохождения контрастного вещества через печень (этот момент обычно наступает к концу ведения препарата). Портография в ряде случаев имеет решающее диагностическое значение, помогает поставить правильный диагноз, оценить возможность дальнейшего лечения.
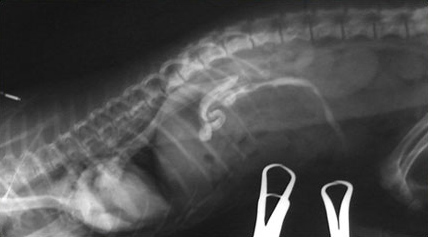 | 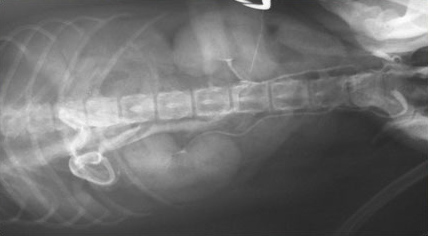 | 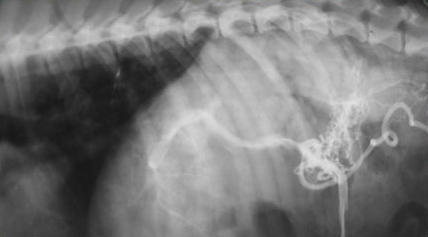 |
| Слева — врожденный портокавальный шунт у собаки йоркширский терьер. В центре — Приобретенный портосистемный шунт у собаки при циррозе печени. Справа — Цирроз печени. | ||
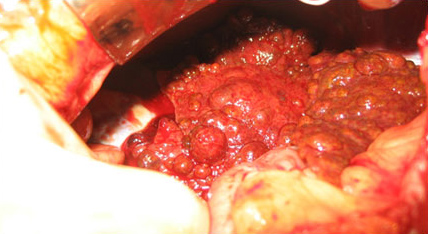
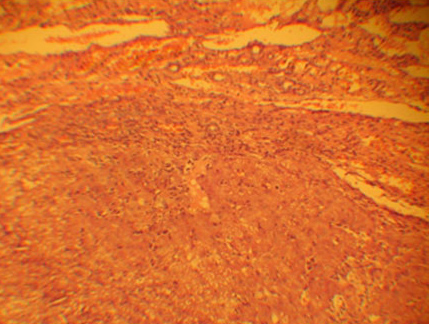 Мульти-монолобулярный постнекротический активный цирроз печени.
Мульти-монолобулярный постнекротический активный цирроз печени.
Ультразвуковая эхография
Исследование с помощью ультразвука используется для идентификации внутрипеченочного шунта и для изучения системы печени и желчного пузыря, а также для исследования почек. В некоторых случаях наличия у собак внутрипеченочного шунта печень имеет малые размеры, вены печени очень малы или совсем неразличимы, а почечная лоханка увеличена. При правильном проведении ультразвуковая диагностика может дать решающие данные для правильного диагностирования гепатоэнцефалопатии.Ядерная сцинтиграфия печени представляет собой неинвазивный метод, пригодный для диагностики, однако его редко используют в повседневной практике.
Биопсия печени
Гистопатологические показатели, полученные из биопсии печени в случае гепатоэнцефалопатии, могут быть неявными. В некоторых случаях при врожденном портокавальном шунте наблюдается отсутствие ветви портальной вены на участке триады. Биопсию печени следует получать для того, чтобы можно было оценить другие проявления гепатопатии, такие как атрофия печени, диффузная жировая инфильтрация, цирроз, либо предциррозное состояние, фиброз, холангиогепатит и идиопатический липидоз у кошек. Иногда гистологическое или даже цитологическое исследование носит решающий характер в диагностике и прогнозе заболевания, так как дает наиболее обьективные данные о морфологии печени, помогает оценить возможности восстановления печени и выбрать правильное лечение.
Цитологическое исследование печени с липидозом
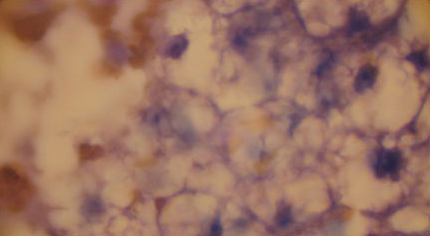 |  | 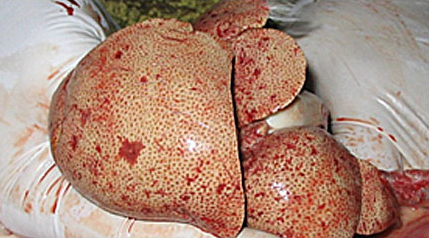 |
| Слева — Цитологическое исследование печени с липидозом. В центре — Цитологическое исследование печени с липидозом Справа — липидоз печени у кошки. | ||
Исследование мочи

Камень в мочевом пузыре у йоркширского терьера с портокавальным врожденным шунтом.
Исследование мочи при подозрении на гепатоэнцефалопатию является обязательным. Присутствие уратов в моче у молодого животного с высокой вероятностью говорит о наличии портокавального шунта и является показанием для проведения портографии. В моче определяются следующие показатели: билирубин, уробилиноген, гемоглобин, кальций, фосфор, микроскопия осадка.
Дифференциальные диагнозы
У молодых животных симптомы, подобные симптомам гепатоэнцефалопатии, могут появляться в случае идиопатической эпилепсии и при заболевании чумой гипокальциемии. Что касается более взрослых собак, то с гепатоэнцефалопатией можно спутать такие заболевания, как энцефалиты, гипогликемия, некоторые токсикозы, метаболические и эндокринные заболевания, уремию. Для того чтобы исключить дифференциальные диагнозы и определить природу нарушений, вызывающих гепатоэнцефалопатию, может оказаться необходимым использование в совокупности всех методов исследования.
Лечение
- Установить и устранить факторы, способствующие развитию гепатоэнцефолопатии.
- Предпринять меры, направленные на снижение и образование, и адсорбцию аммиака и других токсинов, образующихся в толстой кишке, включающих в себя модификацию пищевых белков, изменение кишечной микрофлоры и внутрикишечной среды.
Выбор методов лечения зависит от клинической картины, острой или хронической формы заболевания.
Методы лечения при острой гепатоэнцефолопатии:
- выявить факторы, способствующие возникновению гепатоэнцефолопатии;
- очистить кишечник от азотсодержащих веществ. (дать слабительное, сделать клизму);
- назначить безбелковую диету;
- назначить лактулозу; антибиотики (неомицин, метрогил);
- необходимо поддерживать калорийность пищи, должны быть приняты меры, направленные на восстановление жидкостного и электролитного баланса. Для этого проводят инфузионную терапию (с использованием препаратов гепасол, растворов Рингера, Хартмана.);
- Для лечения используются солкосерил, ноотропные препараты, глюкокортикоиды (метилпреднизолон), препараты, улучшающие реологические свойства крови (стабизол, рефортан).
Методы лечения при хронической энцефалопатии:
- ограничить содержание белка в корме;
- обеспечить опорожнение кишечника 2 раза в сутки
- Закислить содержимое кишечника, для того чтобы уловить аммиак (в виде NH4+) и ускорить его выведение из кишечника. Это достигается назначением лактулозы, которая также может быть использована в качестве безбелкового источника энергии для кишечных микроорганизмов, снижая, таким образом, дальнейшее производство аммиака. Стандартная доза составляет 2,5-5 мл для кошек и 2,5-15 мл для собак 3 раза в день. Недавно было показано, что многообещающие результаты в деле контролирования гепатоэнцефалопатии может обеспечить родственное лактулозе вещество — лактитол, которое принимают в виде порошка;
- при ухудшении состояния переходят на лечение, используемое при острой энцефалопатии.
Окклюзия шунтов
Хирургическое устранение портокавального шунта может привести к регрессу тяжелой портосистемной энцефалопатии. Данный метод лечения можно применять при врожденных и приобретенных портокавальных шунтах.
Лечение собак с гепатопортальной микроваскулярной дисплазией
Как такового специфического лечения при данной патологии не существует.
Прогнозы зависят от степени выраженности клинических симптомов. Первоначально таких больных переводят на кормление с наименее вредными источниками протеинов, растительные и молочные белки, добавляют лактулозу или лактитол.
Собакам со стойкими нейроповеденческими симптомами назначают антибиотики- неомицин, метронидазол. У собак с выраженными симптомами прогноз осторожный вплоть до неблагоприятного. У пациентов с гепатопортальной микроваскулярной дисплазией без симптомов возможен благоприятный прогноз вплоть до отличного. Тем не менее, рекомендуется пожизненное диетическое питание.
Заболевания языка
стоматолог-ортопед, стоматолог-хирург, стоматолог-имплантолог; врач высшей категории, кандидат мед. наук
СЕТЬ РОССИЙСКО-АМЕРИКАНСКИХ СТОМАТОЛОГИЧЕСКИХ КЛИНИК ДЕНТА
Общая информация
Язык – один из важнейших органов человеческого организма, отвечающий не только за вкусовые ощущения, но и за речевой аппарат. Появившийся налёт на языке может означать целый ряд нарушений в работе организма, или же быть признаком серьёзного заболевания.
Заболевания языка подразделяются на десятки типов, и каждый из них требует отдельного изучения, диагностики и своевременного лечения. Запущенные случаи даже самых лёгких форм таких болезней могут привести к необратимым последствиям, влияющим не только на состояние организма в общем, но и на дикцию и даже саму возможность говорить.
Виды и симптомы заболеваний языка
Глоссит
Одно из самых распространённых заболеваний языка – глоссит – является ещё и одним из наиболее трудно вылечиваемых из-за большого процента рецидивов. По факту это воспалительный процесс на языке, вызванный, как внешними факторами (травмы и ожоги), так и изменениями внутри организма (инфекции и последствия перенесённых заболеваний).
На сегодняшний день в медицинской практике выделяется до 11-ти разновидностей глоссита, каждый из которых имеет свою природу, симптоматику, течение и возможные последствия. Также глосситы классифицируются по очагу воспаления – кончик, средняя часть, корень и т.д.
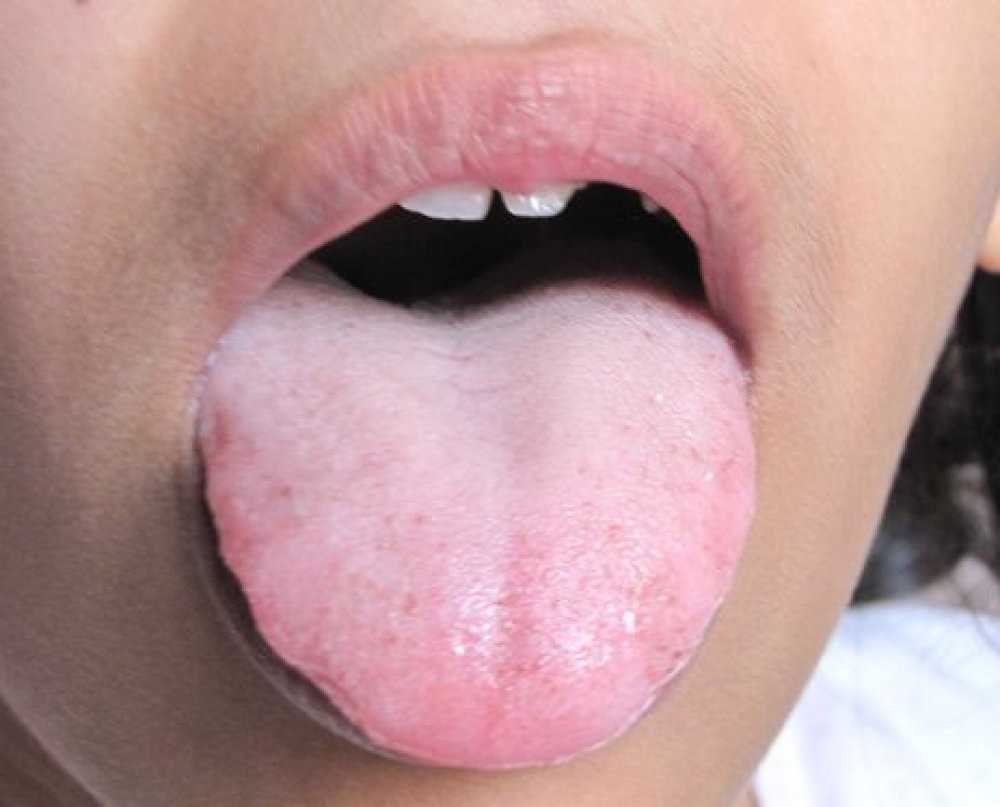
Среди самых распространённых симптомов глоссита врачи выделяют:
- Появление налёта на всей поверхности языка;
- Характерный бледный язык;
- Жжение и отёчность языка;
- Притупление вкусовых ощущений;
- Появление афтозных язвочек;
- Так называемый лакированный язык;
- Обильное слюноотделение;
- Неприятный запах изо рта и др.
Географический язык
Называемый также мигрирующим типом глоссита – географический язык – это заболевание, при котором цвет языка становится неравномерным, покрывая поверхность красными пятнами, окружёнными белыми ореолами, напоминающими рисунок карты – отсюда и название.
В отличие от некоторых видов глоссита, географический язык чаще – симптом других нарушений, а не сама причина. У взрослых появление неравномерных красных пятен на языке означает проблемы с работой желудочно-кишечного тракта, эндокринные расстройства, и сбои в работе кровеносной системы. У маленьких детей географический язык появляется на фоне диатеза.
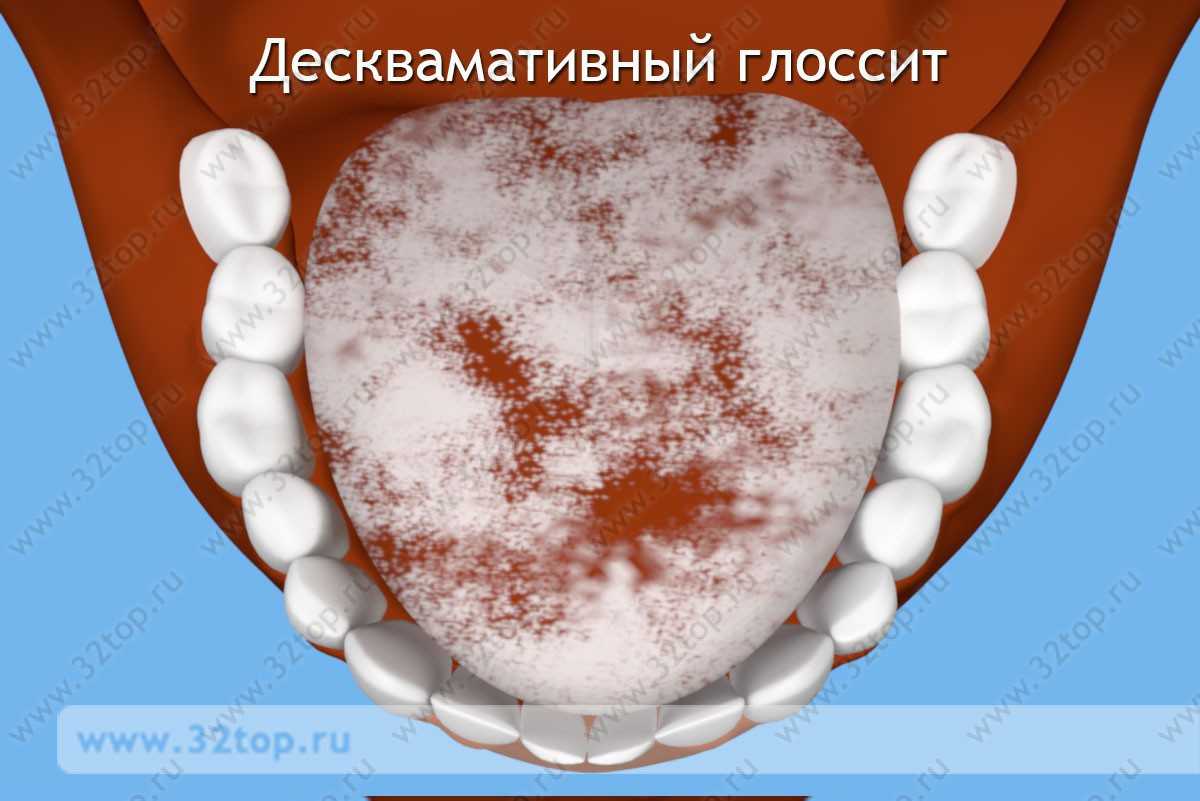
Географический язык развивается при следующих симптомах:
- Резкое опухание средней части языка;
- Появление неестественно белых участков и их вылущивание;
- Лёгкое жжение;
- Возможная затрудненность проглатывания пищи.
Кандидозный стоматит (молочница)
Называемый в большинстве медицинских справочников молочницей, кандидозный стоматит представляет собой серьёзное заболевание не только языка, но и всей полости рта. Подвержены ему в большинстве случаев маленькие дети до 10 лет, но и среди взрослых болезнь периодически диагностируется.
Вызывают заболевания грибки Candida , присутствующие в организме каждого человека, но из-за ослабленного иммунитета и ряда других причин они начинают размножаться слишком быстро, поражая слизистые оболочки.
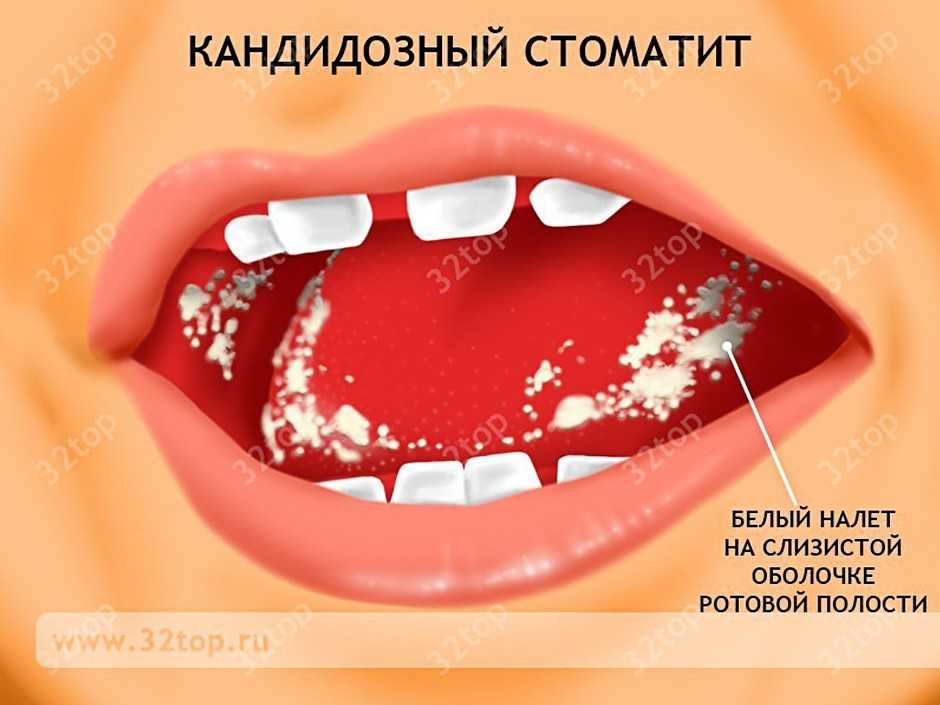
Симптомы кандидозного стоматита почти всегда одинаковы, это:
- Белый налёт на языке, внутренней поверхности щёк и губ;
- На ранних стадиях – равномерно бледный язык;
- Болезненные ощущения при глотании;
- Кровотечения при попытке удалить налёт ватным тампоном;
- Жжение в области налёта;
- Характерный «металлический» привкус слюны;
- Неприятный запах изо рта.
Лейкоплакия
Под лейкоплакией языка и полости рта подразумеваются воспалительные процессы слизистой оболочки, вызывающие ороговение одного или нескольких участков поверхности эпителия. Главные причины возникновения поражений – регулярное физическое раздражение зубными протезами и прочим, а также злоупотребление табаком.
Долгое время лейкоплакия считалась главным признаком развития рака языка, но последние исследования показывают, что даже при запущенном случае заболевания онкология прогрессирует в крайне редких случаях.

К немногочисленным симптомам лейкоплакии относят:
- Появление характерных бляшек белого или светло-серого цвета;
- Возможные эрозийные поражения кожи вокруг бляшек;
- Повышение чувствительности языка к горячей пище и напиткам.
Поскольку болезненных ощущений при лейкоплакии практически не наблюдается, то заболевание может прогрессировать годами.
Красный плоский лишай
Красный плоский лишай – это хроническое заболевание, поражающее язык, полость рта, а также половые органы и ногти. Характеризуется специфическими высыпаниями красного цвета, не имеющими конкретной локализованной зоны. Болезнью страдают в основном представители старшего поколения – от 40 до 60 лет.
Причиной красного лишая часто становится сбой в работе иммунной системы, а также частые стрессы и наличие в организме инфекционных очагов.
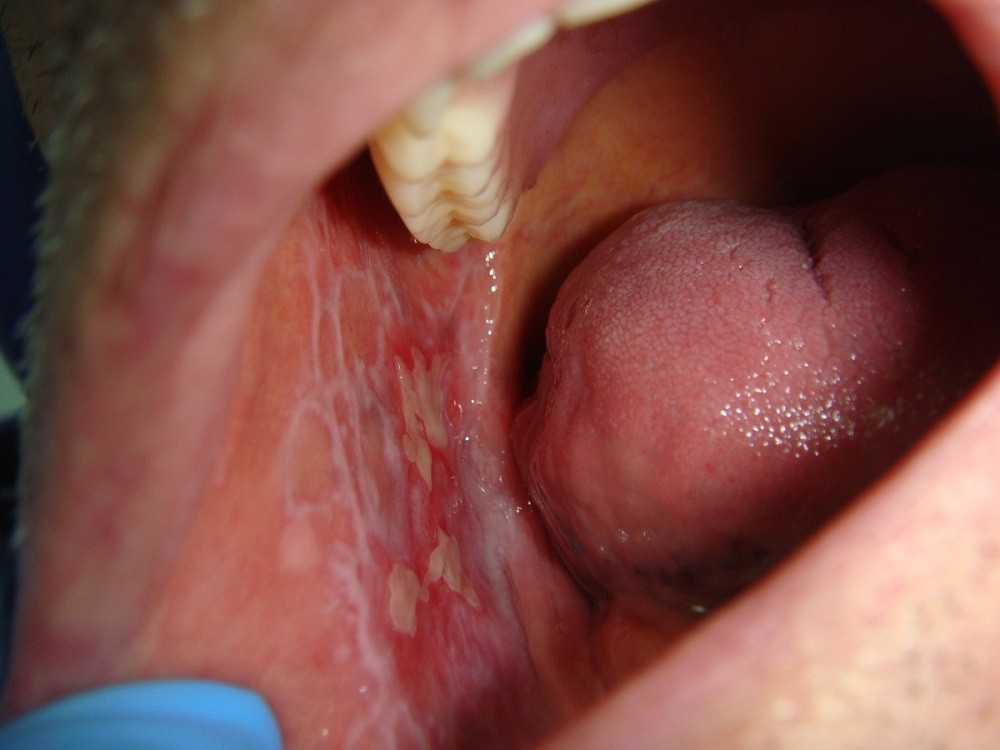
Симптомов красного плоского лишая не так много, это:
- Непрекращающийся зуд, усиливающийся при контакте с зоной поражения;
- Красные точечные высыпания по всей поверхности языка;
- При афтозной форме появляется характерная язва на языке;
- В редких случаях – поражение ногтей.
Причины заболеваний языка
Несмотря на то, что разновидностей заболеваний языка насчитывается порядка нескольких десятков, причины их возникновения во многом схожи. Их условно можно разделить на внешние и внутренние факторы, которые, так или иначе, приводят к возникновению проблемы.
К причинам внешнего порядка относят:
- Травмирование языка и слизистой оболочки слишком твёрдой пищей;
- Частое потребление солёных, острых и слишком жирных продуктов;
- Систематические ожоги горячим чаем/кофе;
- Передозировки лекарственными препаратами;
- Неправильно подобранные зубные протезы;
- Злоупотребление табаком и алкоголем;
- Беспорядочные половые связи.
Однако часто заболевания языка вызываются самыми разными нарушениями работы организма, среди которых:
- Авитаминоз;
- Красная волчанка;
- Любые воспалительные заболевания эпителия;
- ВИЧ, СПИД и сифилис;
- Пневмония;
- Туберкулёз;
- Гастриты и язвенная болезнь;
- Холера;
- Почечная недостаточность и др.
Лечение заболеваний языка
Комплексное лечение любого заболевания языка включает в себя обследование с обязательными анализами крови, биопсией и другими назначенными лечащим врачом пунктами. Если язык поражён вследствие внутреннего сбоя в организме или инфекции, то сначала устраняется ключевая первопричина, и только потом начинается лечение слизистой оболочки.
Говоря об общих рекомендациях стоматологов, занимающихся заболеваниями языка, называются следующие пункты:
- Если болезнь вызвана травмой любого рода, то назначаются полоскания антисептическими растворами на основе хлоргексидина и прочих составов. Болезненные ощущения ослабляются анестезирующими мазями и гелями.
- Если первопричина – инфекционное заболевание, то пациент после обследования получает назначенный курс противовирусного препарата. Без консультации врача такие средства покупать категорически запрещено!
- Если причина в неправильно установленном зубном протезе или пломбе – то решать это нужно, не выходя из кабинета стоматолога.
- Вне зависимости от причины воспалённого языка, пациенту назначается строгая диета, исключающая алкоголь, твёрдую пищу и другие продукты, способные спровоцировать рецидив.
- Самостоятельное лечение дома можно производить только при одобрении врача, и только если речь об обработке поражённой области антисептическим раствором.
Даже в запущенных случаях заболеваний языка оперативное вмешательство считается крайней мерой. Почти всегда, при должном приёме медикаментов и регулярных осмотрах у лечащего врача можно обойтись консервативными методами лечения.
Возможные последствия
Последствия заболеваний языка могут быть самыми тяжёлыми. При недостаточном лечении и не своевременной диагностике, любая из проблем может привести к следующим осложнениям:
- Обширная интоксикация;
- Переход болезни в хроническую неизлечимую форму;
- Развитие заболеваний зубов и воспаление дёсен;
- Нарушение дикции, вплоть до необратимых дефектов;
- Самые разные психологические проблемы из-за дискомфорта во время общения.
каталог стоматологий и стоматологов России
Профилактика
Профилактические меры для гарантированного недопущения появлений заболеваний языка сводятся к простым правилам, соблюдая которые можно оградить себя от множества недугов. В эти правила входят такие пункты:
- Полный отказ от курения;
- Соблюдение предписанной стоматологом диеты, исключающей любые продукты, являющиеся раздражающим или травмирующим фактором;
- Регулярное соблюдение гигиены полости рта, включая ополаскиватели и зубную нить;
- Использование зубной щётки с рабочей поверхностью для языка;
- Посещение стоматолога минимум раз в полгода.
Часто задаваемые вопросы
Любое заболевание языка коснулось хотя бы раз каждого человека, который, в силу ряда причин, мог даже не подозревать о том, что болен. Такие проблемы всегда вызывают живой отклик на самых разных форумах и сайтах, посвящённых стоматологии.
Редакция портала 32топ предлагает ознакомиться с ответами на наиболее частые вопросы, касающиеся этой проблемы.
Вопрос: У меня не первый раз глоссит, и язва на языке покрывается гнойными нарывами. Врач говорит, их нужно оперировать. Есть ли способ этого избежать?
Ответ: Нет, появление нарывов – одна из немногих причин неизбежного хирургического вмешательства. И чем раньше вы это сделаете – тем лучше.
Вопрос: Какие отвары трав рекомендуют врачи для укрепления иммунитета при молочнице?
Ответ: Здесь подойдут любые травы, обладающие общеукрепляющим эффектом – эхинацея, женьшень, зверобой. Единственное условие – обязательно проконсультируйтесь с врачом.
Вопрос: Может ли глоссит поражать половые органы?
Ответ: Глоссит поражает всю систему слизистых оболочек, к которой также относятся и гениталии.
Вопрос: Есть ли риск развития язв при красном лишае на языке?
Ответ: Риск развития язв есть всегда, потому что эта разновидность лишая имеет как минимум 7 форм, в том числе и эрозивную.
https://fitomarket.ru/blog/novosti/naturalnye_gepatoprotektory_top_5_zashchitnikov_pecheni/
https://infovet.ru/lib/gepatologiya/pechenochnaya-entsefalopatiya-gepatoentsefalopatiya/
https://stom.32top.ru/stat/2285/






